A l’aide de deux exemples :
L’infection respiratoire à Virus Respiratoire Syncytial
L’infection respiratoire à Virus Influenza.
1. Le Virus respiratoire syncytial
1-1. Le Virus
1-2. L’épidémiologie de l’infection à VRS
1-3. La physiopathologie de l’infection à VRS
1-4. Les manifestations cliniques liées au VRS
1-5. Le diagnostic virologique de l’infection à VRS
1-6. Le traitement des infections sévères à VRS
2. La grippe et ses virus
2-1. Les virus de la grippe ou virus Influenzae et leurs modifications antigéniques
2-2. La physiopathologie de l’infection grippale
2-3. Les symptômes de la grippe
2-4. Le diagnostic virologique de la grippe
2-5. Le traitement de la grippe
2-6. Points importants
1. LE VIRUS RESPIRATOIRE SYNCYTIAL
Le virus respiratoire syncytial appartient à la famille des Paramyxoviridæ qui comprend 3 genres :
- paramyxovirus avec les virus parainfluenza et le virus des oreillons
- morbillivirus avec le virus de la rougeole
- et pneumovirus avec le virus respiratoire syncytial (VRS)
1-1. Le virus
Le VRS est un virus
- Enveloppé, l’enveloppe virale dérive de la membrane cytoplasmique par bourgeonnement et elle porte des glycoprotéines de surface. Parmi ces glycoprotéines deux ont un rôle majeur : la glycoprotéine G qui permet l’attachement du virus à la cellule hôte et la glycoprotéine F (ou protéine de fusion) qui permet la fusion des membranes cellulaire et cytoplasmique lors de la pénétration virale.
- A capside hélicoïdale
- Et dont le génome est constitué d’une molécule d’ARN
On n’observe pas de variations antigéniques importantes du VRS dans le temps, en tous cas rien qui ressemble aux cassures et glissement des virus de la grippe. Il existe deux groupes antigéniques A et B relativement stables d'où l'absence de pandémie.
1-2. L’épidémiologie
Le VRS est ubiquitaire et se diffuse lors d’épidémie survenant tous les ans durant la saison froide et humide généralement de décembre à mars dans les pays tempérés. Des souches des deux groupes antigéniques circulent de façon concomitante. L’épidémie de VRS précède ou succède à l’épidémie annuelle de grippe, les épidémies à ces deux virus sont en effet rarement concomitantes.
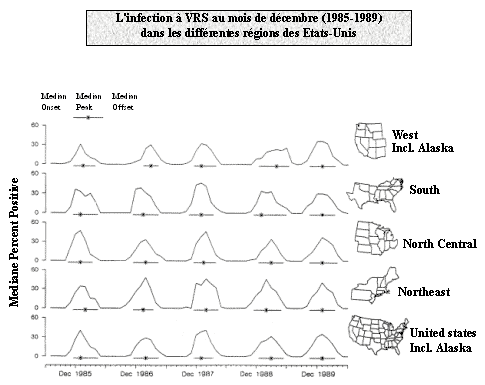
L’infection par le VRS survient très tôt dans l’enfance. Environ 50% des enfants s’infectent avant l’âge de un an et 100% des enfants de 3 ans ont déjà rencontré le virus. Les ré-infections sont fréquentes à tout âge mais particulièrement lors des trois premières années de la vie. Ces ré-infections s’expliquent probablement par une réponse immunitaire qui n’est que partiellement efficace et cumulative.
Le VRS est très contagieux. Sa transmission est essentiellement respiratoire, interhumaine directe par le biais de gouttelettes respiratoires. Cependant, la transmission du VRS peut aussi être manuportée par contact avec une surface contaminée. En effet, le VRS bien qu’assez fragile peut survivre 30 minutes sur la peau, 7 heures sur les surfaces et 40 minutes sur une blouse. En l’absence du respect des règles d’hygiène le virus peut être responsable d’infections nosocomiales en diffusant de patients à patients ou de soignants à patients.
1-3. La physiopathologie de l’infection à VRS
Dans l'organisme infecté, le VRS entré par inhalation, se multiplie dans l'épithélium respiratoire. L’incubation de l’infection est de 4 à 5 jours. Le VRS se multiplie dans le naso-pharynx et atteint l’arbre respiratoire inférieur probablement par diffusion de cellules à cellules. L'infection par le VRS reste localisée à l'arbre respiratoire, sans virémie, d'où une maladie locale à incubation courte, respiratoire haute ou basse.
Lors de la bronchiolite à VRS on constate :
- une destruction des cellules épithéliales ciliées
- des infiltrats péri-bronchiques de lymphocytes et macrophages
- un œdème de la sous muqueuse avec une sécrétion excessive de mucus.
Ces anomalies sont responsables d’une obstruction des petites bronchioles et de la survenue de la bronchiolite.
La réaction immunitaire dirigée contre le VRS associe :
- une réaction humorale :
* une réponse locale avec synthèse d’IgA sécrétoires dont le rôle est très important
* une réponse systémique avec des anticorps neutralisants.
La réponse humorale locale et générale est protectrice, en effet l’injection d’immunoglobulines spécifiques protége de l’infection.
- une réaction immunitaire cellulaire :
qui jouerait un rôle important dans la défense contre l’infection. En effet, les patients ayant un déficit de l’immunité cellulaire (sujets greffés ou VIH) font des infections à VRS sévères.
Les anomalies présentes lors de l’infection à VRS s’expliquent :
- par un effet cytopathique direct du VRS sur les cellules bronchiques
- par une réaction immuno-pathologique :
La mise en évidence d’un effet immuno-pathogène lors de l’infection virale remonte aux années 1960 lorsque des essais vaccinaux réalisés avec des préparations vaccinales contenant du virus inactivé ont été un échec complet. En effet, ces vaccins étaient administrés par voie générale et entraînaient une très forte réponse immunitaire humorale et cellulaire systémique mais aucune réponse immunitaire locale. Si bien, que lorsque l’enfant vacciné rencontrait le virus la séquence suivant d’événements se produisait :
- Le VRS se multipliait dans les cellules de la muqueuse bronchique non protégée par des IgA sécrétoires,
- Cette infection locale entraînait l’afflux de cellules immunitaires systémiques dont des cellules T cytotoxiques ( CD4) spécifiques du VRS entraînant une destruction très importante des cellules bronchiques infectées.
1-4. Les manifestations cliniques liées au VRS
Le VRS donne des infections localisées à l'arbre respiratoire, particulièrement chez le tout jeune enfant. Les trois-quarts des bronchiolites du nourrisson sont dues au VRS. Ce virus donne aussi des pneumonies du nourrisson. Chez certains nourrissons, en particulier les prématurés, elles sont très sévères, entraînant une insuffisance respiratoire aiguë qui oblige à des mesures de réanimation.
La mortalité des bronchiolites hospitalisées en réanimation pédiatrique est de 2 %.
Par ailleurs, une infection à VRS est souvent retrouvée dans les poumons lors de l'autopsie de nourrissons morts subitement. L'infection à VRS n’est probablement qu’un facteur déclenchant parmi d'autres des morts subites du nourrisson.
Le VRS donne aussi des réinfections chez les adultes en contact avec de jeunes enfants. Mais ces adultes, sauf état d'immunodépression, ne font habituellement qu'une infection respiratoire bénigne. Une infection sévère peut s’observer chez les adultes imunodéprimés ou chez les vieillards où la période d'épidémie à VRS est à l'origine d'un excès de mortalité.
L'infection à VRS pose donc, comme la grippe, un très sérieux problème de santé publique.
1-5. Le diagnostic virologique de l’infection à VRS
La mise en évidence du virus n’est pas fait systématiquement car le diagnostic est essentiellement clinique. Cependant, dans les formes sévères en particulier celles pour lesquelles l’enfant sera hospitalisé, il est intéressant de faire le diagnostic virologique.
Le prélèvement de choix pour la mise en évidence d’un virus respiratoire est l’aspiration naso-pharyngée. Un écouvillonnage par grattage énergique de la paroi nasale peut aussi être réalisé, l’écouvillon sera alors déchargé dans un tube contenant un milieu de transport virologique. Une aspiration trachéale ou bronchique peut aussi être réalisée chez des enfants intubés.
La technique de choix pour le diagnostic virologique est l’immunocytodiagnostic rapide.
- La technique d’immunofluorescence directe est très souvent utilisée et permet de faire le diagnostic d’infection à VRS en une heure:
des cellules des sécrétions respiratoires sont étalées sur une lame et mises en contact avec un anticorps spécifique anti-VRS marqué par un fluorochrome. La lecture au microscope à fluorescence révèle la présence d’une fluorescence cytoplasmique des cellules bronchiques traduisant la présence du VRS. - des techniques immunoenzymatiques peuvent aussi être utilisées. Des techniques ultra rapides (en quelques minutes) qui utilisent le principe de l’immunofiltration sur membrane ("savonnette") sont aussi disponibles dans le commerce.
Le prélèvement respiratoire peut aussi être mis en culture pour la recherche du VRS. Le virus se multiplie en culture de cellules courantes en donnant des syncytiums (comme son nom l'indique) avec inclusions cytoplasmiques.
Le sérodiagnostic n’a pas d’intérêt car la séroconversion est inconstante et de toute façon toujours tardive, à la convalescence.
Il faut donc privilégier le diagnostic rapide qui est très fiable.
1-6. Le traitement des infections sévères à VRS
Les infections respiratoires sévères à VRS ont fait l’objet de traitements par aérosol de Ribavirine, nucléoside antiviral à spectre large. L’efficacité de ce traitement est discutée et en pratique il est réservé aux formes très sévères d’infection à VRS.
Un vaccin contre le VRS serait très utile. Malheureusement il n’y a aucun vaccin efficace actuellement disponible.
Des anticorps monoclonaux humanisés dirigés contre un épitope de la protéine de fusion du VRS sont commercialisés (Palivizumab). Chez des enfants à haut risque, l’administation mensuelle de ces anticorps pendant toute la période épidémique réduit de plus de 50% l’incidence des hospitalisations liées au VRS. Ces préparations d’anticorps dont le coût est très élevé, sont réservées exclusivement aux enfants à haut risque de développer une infection sévère à VRS, c’est à dire les nourrissons de moins de 6 mois nés prématurément ou les enfants de moins de 2 ans ayant une dysplasie bronchopulmonaire.
2. LA GRIPPE ET SES VIRUS
La grippe est une infection virale souvent bénigne et très fréquente. La plupart des sujets font plusieurs fois la grippe dans leur vie. Cependant la grippe peut tuer : l'épidémie de 1918 a fait 100 millions de morts, soit 1% de la population mondiale et 5 fois plus de victimes que la première guerre mondiale.
2-1. Les virus de la grippe ou virus influenzae et leur modifications antigéniques
A.Morphologie des virus influenzae
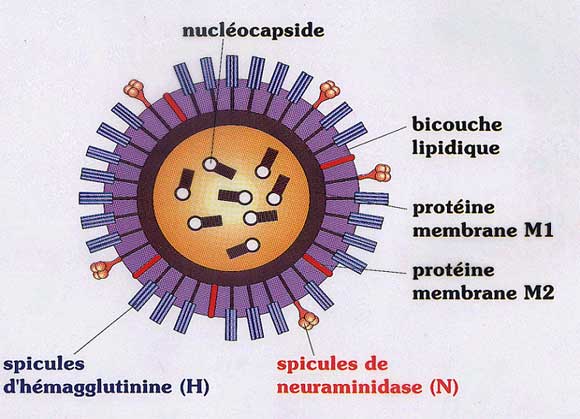
- Les virus influenza appartiennent à la famille des orthomyxoviridae.
- Les virus de la grippe ont une enveloppe dérivée de la membrane cytoplasmique. L’enveloppe porte deux sortes de spicules, qui sont des glycoprotéines virales : les spicules d'hémagglutinine, en abrégé HA, et des spicules de neuraminidase, en abrégé NA. Ce sont des antigènes viraux. Ces structures jouent un rôle dans la multiplication virale. L'hémagglutinine, au niveau de l'attachement du virus sur la membrane cytoplasmique des cellules à infecter et au niveau de la fusion de l’enveloppe à la membrane cytoplasmique. La neuramidase joue un rôle au moment du détachement des bourgeons lors de la formation des nouveaux virus et d'autre part elle lyse le mucus bronchique qui a des propriétés antivirales. On décrit plusieurs sous types d’HA ou de NA selon les virus, à ce jour 15 sous types d’HA et 9 sous types de NA sont connus.
- La face interne de l’enveloppe est tapissée d’une membrane interne composée de deux protéines de membrane M1 et M2.
- La nucléocapside à symétrie hélicoïdale est composée de 8 segments distincts d’ARN associées à des sous-unités protéiques, la fragmentation du génome viral favorise les réassortiments génétiques.
Il existe trois types de virus grippaux distincts par leurs protéines de capside : les virus influenza A, les virus influenza B et les virus influenza C (ces derniers pour mémoire, car ils ne donnent pratiquement que des infections inapparentes). La nomenclature des souches est la suivante : les souches sont donc appelées A ou B, l’hôte d’origine est indiqué pour les souches d’origine non humaine, puis l’origine géographique, le numéro de la souche, l’année d’isolement et le sous type d’HA et de NA. Exemples d’une souche humaine A/ Singapore/1/57 (H2N2), d’une souche aviaire : A/Hav/Hong-Kong/
B. Les variations antigéniques :
- Les antigènes grippaux :
L'hémagglutinine est très immunogène et provoque l’élaboration d’anticorps neutralisants le pouvoir infectieux du virus. Ces anticorps protecteurs sont spécifiques de sous-types et de variants. Les anticorps se maintiennent pendant des années. Lors des réinfections par des virus apparentés, on observe une réponse immunitaire de type rappel.
La neuraminidase est moins immunogène que l’HA. Elle induit des anticorps non neutralisants mais qui protégent contre les manifestations cliniques de la grippe sans inhiber l’infection biologique.
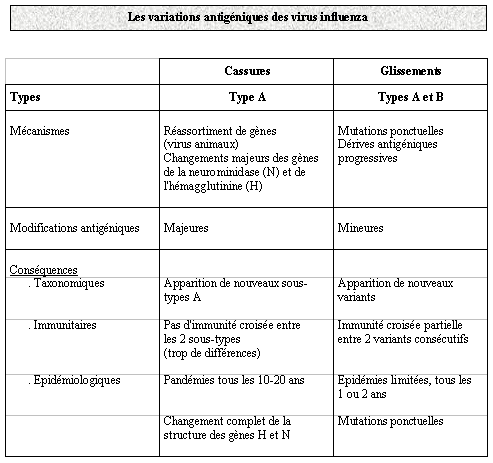
- Les glissements et les sauts antigéniques :
Après une épidémie de grippe, l'hiver suivant, la plupart des sujets ont des anticorps anti-HA ou anti-NA. Cela crée dans la population humaine une barrière immunitaire vis-à-vis du virus de l'épidémie précédente. C'est alors que les virus influenza démontrent leur faculté d'adaptation, surtout les virus influenza A. Quelque part dans le monde, en Chine Centrale le plus souvent, il apparaît un mutant, un virus influenza A nouveau qui va pouvoir surmonter la barrière immunitaire, grâce à une modification antigénique de la neuraminidase ou de l'hémagglutinine.
Ces modifications par mutation comportent deux degrés, des mutations radicales qui changent complètement la constitution antigénique de la neuraminidase ou de l'hémagglutinine et des modifications plus légères.
- Les modifications radicales sont ce qu'on appelle une "cassure" ou “ saut ” antigénique. Ainsi les premiers virus influenza A isolés en 1933 avaient une hémagglutinine H0, une neuramidase N0. En 1947, est apparu un virus influenza A H1, N1. En 1957, un virus influenza A H2, N2 (grippe asiatique). En 1968, un virus influenza A H3, N2 (grippe de Hong Kong).
Ces modifications antigéniques majeures de la neuraminidase ou de l'hémagglutinine ne concerne que les virus de type A, et ont fait apparaître, à l'intérieur des virus de type A autant de sous-types différents, chaque sous-type nouveau remplaçant dans la population le sous-type précédent et créant une pandémie (épidémie de toute ou quasiment toute la population mondiale), puisque le virus est radicalement nouveau pour la population mondiale. Ainsi la dernière pandémie a été celle de Hong Kong en 1968.
- D'autre part entre chaque saut antigénique se produit un deuxième type de modification antigénique, qui modifie légèrement la neuraminidase N ou l'hémagglutinine H. C'est un glissement antigénique survenant tous les ans ou tous les deux ans. Ces modifications antigéniques mineures donnent non pas des pandémies mais tous les ans ou tous les deux ans, des épidémies limitées touchant une fraction seulement de la population. Ce glissement antigénique aboutit tout de même au fait que la souche de grippe H3 N2 de l'hiver 94-95 par exemple, est notablement différente de la souche H3 N2 initiale apparue en 1968. Le glissement antigénique concerne le virus influenza A et le virus influenza B. Le glissement antigénique détermine l'apparition de nouveaux variants, alors que les sauts donnent de nouveaux sous-types.
- L’origine des modifications antigéniques des virus grippaux :
Les glissements antigéniques, modifications mineures sont favorisées par l'instabilité génétique du RNA (par opposition au DNA) et le caractère infidèle des RNA polymérases virales (pas de mécanisme de relecture ni de correction d'erreur). Ils résultent du changement ponctuel de quelques bases nucléiques dans le gène correspondant à l'hémagglutinine ou/et le gène correspondant à la neuraminidase. Par glissement apparaissent à l'intérieur du même sous-type, H3N2 par exemple, toute une série de variants qui s'éloignent progressivement de la souche d'origine : les variants H3 N2 actuels sont très différents de la souche H3 N2 initiale apparue en 1968.
Les cassures antigéniques ou sauts correspondent à des remaniements génétiques beaucoup plus importants que des mutations ponctuelles. Ce sont des "réassortiments" génétiques, c'est à dire des échanges complets de gènes entiers. Ces échanges portant sur les gènes de l'hémagglutinine et/ou de la neuraminidase se font avec des virus influenza animaux, des porcs, des chevaux, des oiseaux aquatiques (canards). Les sauts aboutissent à l'apparition de nouveaux sous-types à l'intérieur du type A. Le réservoir des virus influenza A est constitué par les oiseaux aquatiques. Le porc, qui a des récepteurs à la fois pour les virus influenza A aviaires et pour les virus influenza A humains, est un hôte intermédiaire où se font les réassortiments génétiques. Les nouveaux sous-type A et donc les nouvelles pandémies naissent généralement en Chine rurale où voisinent à l'étroit hommes, cochons et canards. Cependant, des passages directs de souches aviaires à l'homme sont possibles (grippe du poulet à Hong Kong en 1997 puis 1999) mais ne donnent pas d’épidémie importante car ils restent mal adaptés à l’homme.
Il n'y a pas de virus influenza B animaux et donc pas de sauts pour les virus influenza B humains qui ne font que glisser.
Une grande question à 2 volets : à quand la prochaine pandémie inévitable et quelle en sera la gravité (comme en 1918 ou comme en 1968 seulement ?). La grippe du poulet à virus A H5N2 qui en 1997 a donné quelques cas d’infections humaines mortelles à Hong-Kong a fait très peur au début. Mais, ses capacités épidémiologiques chez l’homme se sont en fait révélées très limitées.
2-2. La physiopathologie de l’infection grippale
Le virus pénètre par le nez et la gorge par inhalation de gouttelettes en suspension dans l’air et se multiplie aussitôt dans l'arbre respiratoire cilié qui va du nez jusqu'aux bronchioles.
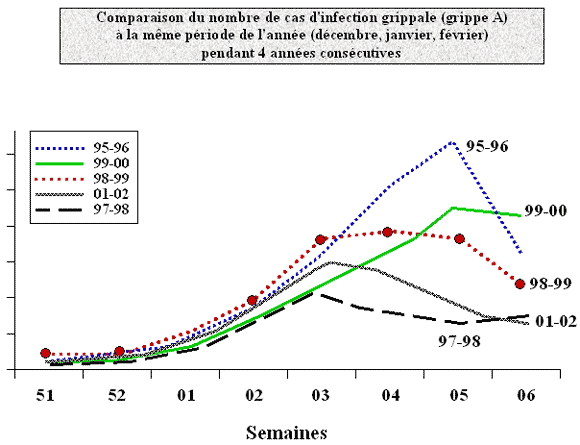
L'infection ne va pas au-delà, dans les formes habituelles. Le virus ne se multiplie pas dans l'alvéole. En profondeur il ne dépasse pas la membrane basale. Sauf exception, il n'y a pas de virémie. Donc la multiplication virale reste localisée à la porte d'entrée du virus dans l'organisme. D'où la brièveté de l'incubation, 1 à 3 jours. Cette multiplication locale donne une nécrose de l'épithélium respiratoire cilié, donc des lésions intenses, mais réversibles. Cette nécrose s'accompagne d'hypersécrétion de mucus bronchique et d'une hypertension modérée dans la petite circulation.
Cette nécrose explique la toux, l'épistaxis inconstante, et les signes généraux intenses. Il est habituel qu'une nécrose tissulaire donne de la fièvre et de plus ici, les protéines virales par elles-mêmes sont pyrogènes. Mais dans tout cela, il n'y a pas de diffusion du virus, la grippe est le type même des maladies virales locales. On pense que fièvre et myalgies sont dues à la sécrétion de cytokines : d'interféron (l'administration médicale d'interféron donne de fait une fièvre brutale et des myalgies pseudogrippales) et d’interleukine 6.
2-3. Les symptômes de la grippe
A noter que l’infection par les virus grippaux est fréquemment asymptomatique.
A. La grippe non compliquée
C'est une maladie qui sévit l'hiver. Chaque hiver survient une épidémie de grippe avec tous les 10 ans environ une épidémie d'une étendue très inhabituelle qui touche pratiquement toute la population mondiale : on parle alors de pandémie. Il en était ainsi en 1947, en 1957 et en 1968. Le mot influenza, d'origine italienne, rappelle qu'autrefois on croyait que la grippe survenait sous l'influence des astres.
Le mot grippe vient d'agrippé et suggère une maladie brutale. De fait, après une incubation de 1 à 2 jours c'est une fièvre brutale à 40°C accompagnée de douleurs diffuses, de céphalées, de rachialgies, de myalgies.
Il existe des signes respiratoires, mais ils sont discrets : un écoulement nasal, une toux sèche, parfois des douleurs pharyngées, laryngées, trachéales, ou un saignement de nez (une épistaxis).
Chez le jeune enfant une fièvre de cette intensité peut déclencher une crise convulsive hyperpyrétique.
L'examen physique est habituellement négatif, contrastant avec l'intensité des signes généraux. L'auscultation pulmonaire est le plus souvent normale. La radiographie pulmonaire également. On ne trouve de foyer pulmonaire que dans 10 % des cas. Il ne faut donc pas compter sur la radiographie pulmonaire pour confirmer un diagnostic de grippe.
3 à 4 jours plus tard tout est rentré dans l'ordre, la fièvre a disparu, du moins dans les formes simples. Donc la grippe donne un syndrome fébrile de durée limitée qui ressemble à la phase d'invasion de bon nombre de maladies infectieuses.
Comment faire le diagnostic de grippe en pratique?
En effet, les signes cliniques sont non spécifiques. Le diagnostic clinique de la grippe repose sur des arguments épidémiologiques très simples : c'est l'hiver, et l'on a appris par les médias qu'il y avait une épidémie de grippe, épidémie apparue en général en Orient (Chine), et qui, à un endroit donné, dure en moyenne 6 semaines. On sait en effet cela grâce à un réseau de surveillance de la grippe, placé sous l'égide de l'O.M.S., avec comme relais local le Centre National de la Grippe de l'Institut Pasteur de Paris, pour le Nord de la France, celui de Lyon pour le Sud. Il s'appuie sur un réseau-sentinelle mobilisant des volontaires Pédiatres et Généralistes surveillant particulièrement les collectivités d'enfants qui ont un rôle d'amplificateur pour la propagation des virus de la grippe.
B. Les complications de la grippe
La grippe est responsable d’un excès de morbidité et d’une surmortalité. On estime la mortalité moyenne de la grippe à 0,1 %. Cette surmorbidité et surmortalité sont liées :
- La surinfection bactérienne :
La grippe se complique fréquemment d’infections ORL en particulier d’otite moyenne aiguë chez l’enfant.
La grippe peut se compliquer d’une pneumopathie bactérienne. En effet, la nécrose de l'épithélium respiratoire cilié et l'hypersécrétion de mucus font de l'arbre respiratoire l'équivalent d'un tube de culture pour bactéries, d'autant plus que les macrophages infectés par les virus grippaux ont un pouvoir phagocytaire diminué. D'où la possibilité de surinfection à Haemophilus influenza, Staphylococcus aureus, Streptococcus pneumoniae, Neisseria, c'est-à-dire des bactéries commensales de l'arbre respiratoire supérieur qui profitent de la grippe pour "faire une descente" dans l’arbre respiratoire inférieur, normalement stérile. C'est en cas de surinfection bactérienne que l'on voit le classique V grippal de la courbe thermique et une hyperleucocytose à polynucléaires. La pneumonie à Staphylococcus aureus est la surinfection la plus grave (mortalité de 30 à 50 %). Cette surinfection bactérienne, qui est difficile à prévoir, n'explique qu'une proportion des morts par grippe.
- La pneumopathie virale maligne, qui associe à la nécrose de la muqueuse respiratoire ciliée, un œdème hémorragique massif qui remplit complètement les alvéoles, distend les poumons : les poumons sont véritablement noyés. On connaît des circonstances qui favorisent l'apparition de cette pneumonie grippale maligne : ce sont tous les états d'insuffisance cardiaque ou respiratoire : les bronchites chroniques de l'adulte, la dilatation des bronches ou la mucoviscidose de l'enfant, les cardiopathies du sujet âgé ou les malformations cardiaques congénitales de l'enfant. Ces sujets fragiles situés aux deux extrêmes de la vie supportent mal l'hypersécrétion bronchique et la surcharge modérée de la petite circulation qui accompagnent l'infection grippale. La sécrétion inappropriée de cytokines est également tenue pour responsable de la grippe maligne
Un autre groupe de sujets risque plus que les autres la grippe maligne : ce sont les femmes enceintes qui ont à l'état physiologique en cours de grossesse, une surcharge de la petite circulation. Il reste que bon nombre de pneumonies grippales mortelles surviennent sans cause favorisante connue, chez des sujets en pleine force de l'âge, sans explication.
2-4. Le diagnostic virologique de la grippe
- Le diagnostic direct :
Il est réalisé à partir des sécrétions nasales prélevées au tout début de l'évolution, par aspiration naso-pharyngée ou à défaut par écouvillonnage de la paroi nasale. Ces virus sont fragiles, d'où l'importance du milieu de transport.
- L'inoculation pour isolement se fait sur culture cellulaire, mais pas sur n'importe quelle culture de cellules, par exemple sur cellules MDCK. Un autre système cellulaire utilisable est représenté par l'oeuf de poule embryonné, inoculé dans la cavité amniotique, c'est-à-dire dans la poche où débouchent les voies respiratoires de l'embryon.
La multiplication virale est décelée par l'apparition d'une hémagglutinine dans le liquide de culture, dans le liquide amniotique, et les virus influenza sont typés très facilement en inhibition de l'hémagglutination (IHA) ou par immunofluorescence.
- Une autre façon de détecter le virus consiste à détecter des antigènes viraux. Il existe des méthodes d’immunocytodiagnostic rapide, consistant à rechercher dans les cellules desquamées du tractus respiratoire l’existence d'une fluorescence à l'aide d'immunsérums antivirus influenza A ou B conjugués à la fluorescéine. On peut également recourir sur les sécrétions respiratoires à une technique immunoenzymatique, soit classique sur support solide (ELISA), soit ultrarapide sur une membrane filtrante (“savonnette”).
- La détection d'acides nucléiques viraux, par RT-PCR par exemple, est une méthode très sensible mais encore réservée actuellement à des laboratoires très spécialisés.
- Le diagnostic sérologique indirect :
Le sérodiagnostic doit porter sur une paire de sérums, S1 prélevé le plus tôt possible la première fois où l'on voit le malade, et S2 prélevé trois semaines plus tard. Un délai de 2 semaines est insuffisant pour une maladie à incubation courte. On recherche une élévation du taux des anticorps d'au moins 1 à 4 à l'examen simultané de deux sérums. Le résultat du sérodiagnostic parvient donc toujours au moment de la convalescence, d'où son absence d'intérêt pour le patient. Rappelons qu'un sérodiagnostic portant sur un seul sérum n'a aucune valeur diagnostique d'infection actuelle; il n'a d'intérêt qu'épidémiologique.
Dans le cas de la grippe il faut privilégier l'isolement et le diagnostic rapide.
- Les indications du diagnostic virologique de la grippe :
Quand est-il intéressant de faire un diagnostic virologique exact par examen de laboratoire, au cours de la grippe? D'abord dans toutes les formes graves. Mais aussi dans les formes banales il est nécessaire de procéder sur quelques cas à l'isolement du virus, cela dans une optique épidémiologique, pour étudier les modifications antigéniques éventuelles au Centre National de la Grippe de l'Institut Pasteur de Paris ou celui, de Lyon et pour actualiser les vaccins. Enfin, quand les cliniciens font une étude particulière à visée cognitive, par exemple, l'étude de l'efficacité d'un vaccin antigrippal ou d'une chimiothérapie antivirale, il faut pour que les conclusions de telles études soient valables, que le diagnostic de grippe soit confirmé et seul le laboratoire peut apporter cette confirmation.
2-5. Le traitement de la grippe
A. le traitement préventif : la vaccination
- Les composants du vaccin
Depuis 1977 circulent, en France et ailleurs, simultanément 3 sortes de souches de virus grippaux.
- des souches de grippe A, H3N2, variants très éloignés de la souche d'origine de 1968
- des souches de grippe A H1N1 qui, comme les souches H3N2, “glissent” tous les ans ou tous les 2 ans.
- des souches de grippe B, qui “glissent” plus lentement.
Il faut donc que les vaccins grippaux soient trivalents. On dispose donc d'un vaccin tué qui contient les deux variants récents de virus grippal A (H1N1 et H3N2 en 1995) et une souche récente de virus grippal B. Pour la fabrication des vaccins, c'est-à-dire pour se protéger d'une épidémie, il faudrait que la souche de virus contenue dans le vaccin soit la souche de l'épidémie, mais c'est difficile en pratique car on n'a souvent pas le temps au cours de l'hiver d'isoler la souche épidémique, de l'identifier, de préparer le vaccin, de le contrôler et de le diffuser à toute la population susceptible d'être atteinte. Ces opérations mènent généralement au mois de Mars et l'épidémie est passée. Pendant l'année du saut on est en manque de vaccin efficace.
En pratique le vaccin contient la souche de l'épidémie précédente qui protège partiellement pour l'hiver suivant, à condition qu'il n'y ait pas eu entre-temps de saut antigénique. En cas de saut antigénique, les vaccins dont on dispose sont complètement périmés.
- L’efficacité de la vaccination
La vaccination n'est pas parfaite. Son taux de protection a été évalué entre 40 et 80 %, ce qui n'est pas à négliger. Son efficacité est limitée (bien que réelle) pour deux raisons. Le vaccin se trouve toujours "en retard d'une mutation" et si cette mutation donne une cassure, le vaccin disponible ne vaut plus rien. D'autre part, c'est un vaccin qui, injecté, par voie sous-cutanée ou IM, suscite surtout des anticorps dans le sang, et peu d'IgA dans les sécrétions respiratoires. Donc il protège mal la seule zone où les virus grippaux se multiplient, c'est-à-dire l'épithélium respiratoire cilié. Enfin, il faut recommencer la vaccination tous les ans, car la protection apportée est brève, et de toutes façons le virus change tous les deux ans.
- Le protocole de vaccination
La vaccination anti-grippale n'est pas obligatoire. Elle est cependant conseillée chez des sujets à risque que sont les insuffisants cardiaques et les insuffisants respiratoires chroniques de tous âges (le jeune enfant atteint de mucoviscidose comme le sujet d'âge mûr atteint d'emphysème, le jeune atteint de cardiopathie congénitale comme l'adulte atteint de cardiopathie dégénérative), les sujets fragiles (transplantés, dialysés …), les vieillards, et les femmes enceintes... et tous ceux qui la demandent pour tenter d’éviter la grippe. La vaccination des personnels soignant des sujets fragiles est tout à fait recommandée dans l'intérêt de ces derniers, il a été montré qu’une telle vaccination du personnel diminuait la mortalité par grippe des sujets fragiles dans certaines communautés (maison de retraite, hôpital).
L'avenir de la vaccination est peut-être dans des préparations antigéniques élaborées pour administration par voie nasale. Un vaccin vivant par souche atténuée après passages en culture de cellules à 25°C (souche adaptée au froid) est à l'essai en administration par voie nasale.
B. Le traitement curatif : les anti-viraux
- La Rimantadine
C'est une substance antivirale qui agit sur la pénétration et la décapsidation des virus, par voie orale. Sa cible est la protéine de matrice M2 qui tapisse intérieurement l'enveloppe virale. Elle est active sur les souches de grippe A mais non de grippe B et surtout à titre préventif. Ce produit peut donner des syndromes dépressifs et des troubles du sommeil et des troubles de la marche, en particulier chez les personnes âgées..
Les virus de la grippe A, en raison du manque de fidélité de la RNA polymérase virale sélectionnent aisément des mutants résistants à la rimantadine. Cela joint aux effets secondaires et à des ventes modestes a fait arrêter la commercialisation du produit.
- Le Zanamivir et l’Oseltamivir
Ce sont des inhibiteurs de la neuraminidase des virus de la grippe A comme de la grippe B. Le Zanamivir est administré en pulvérisation par voie et l'Oseltamivir per os.
Ces inhibiteurs de la neuraminidase réduisent la durée de la grippe et l’acuité des symptômes si elles sont administrées dans les 24-48 premières heures de la maladie et sont actives en traitement prophylactique. Dans ce cas le traitement se fait en cas de contage ou tant que dure la vague épidémique.
Ces molécules sont très bien tolérés en dehors d’un risque de bronchospasme pour le Zanamivir chez les personnes asthmatiques). Il n’y a pas de résistances cliniques décrites après plus de trois années d’utilisation.
L’utilisation des inhibiteurs de la neuraminidase serait particulièrement intéressante dans le cas d’apparition d’un variant pandémique non reconnu par les vaccins.
2-6. Points importants
- La grippe A et la grippe B sont dûes à des virus à RNA segmenté, chaque segment correspond à un gène. Ils sont enveloppés et portent deux sortes de spicules glycoprotéiques, l'hémagglutinine et la neuraminidase qui toutes deux suscitent des anticorps protecteurs.
- La grippe est une infection virale localisée à l'épithélium respiratoire cilié, peu accessible à la vaccination.
- D'autant que les virus grippaux sont sujets à des variations antigéniques : sauts pour les virus influenza A et glissements pour les virus influenza A et B.
- Les sauts ont pour origine des réassortiments de gènes entre souches de virus influenza A humains et animaux.
- Les réseaux de surveillance épidémiologique de la grippe pour isolement et caractérisation des nouvelles souches sont indispensables à la préparation de vaccins actualisés.
- Ceux-ci sont trivalents (AH3N2, AH1N1 et B), à administrer tous les ans aux sujets fragiles.
|
|
|
|
|
