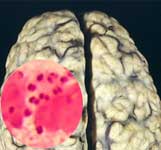
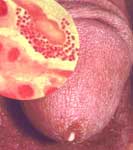
| Le genre Neisseria se caractérise par un aspect morphologique particulier: Diplocoque à Gram négatif se présentant sous la forme de grains de café ou diplocoque à face aplatie, par ailleurs aérobie strict. Plusieurs espèces commensales peuvent être isolées au sein de la flore oropharyngée de l'homme. Deux espèces pathogènes sont bien individualisées : N. meningitidis, agent régulièrement identifié lors de cas de méningite cérébrospinale (1 cas pour 100.000 habitants/an en France) et N.gonorrhoeae, agent de la gonococcie, de la blennorragie ou encore de la gonorrhée. Cette maladie vénérienne en régression en France peut entrainer de graves complications chez la femme. |
NEISSERIA MENINGITIDIS
Cette espèce bactérienne encore dénommée méningocoque est l'agent de la méningite cérébrospinale.
A - LES CARACTÈRES DE LA BACTÉRIE
- Cocci à Gram négatif aérobie strict
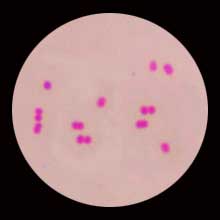
- Phylogénétiquement très proche de N. gonorrhoeae
- Germe fragile (froid, dessiccation) aussi il conviendra de transporter les prélèvements très rapidement au laboratoire
|
- Croissance à 37°C en présence de CO2 après souvent 48 h d'incubation, nécessite des milieux riches tels la gélose "chocolat", en fait au sang cuit ...). L'identification de cette espèce est biochimique après 24 h d'incubation à 37°C. - La présence d'une capsule polysaccharidique permet de distinguer 13 sérogroupes A, B, C, X, Y, W135... Le polysaccharide capsulaire purifié est à la base du principe vaccinal actuellement disponible. Ce vaccin n'est disponible que pour les sérogroupes A, C, et éventuellement W135. Le polysaccharide de type B n'est pas immunogène, car un sucre identique est présent au niveau du cerveau. Les polysaccarides A et C ne sont pas immunogènes avant 18 mois. Le polysaccharide C a récemment été conjugué à un peptide "carrier", permettant une vaccination contre le sérogroupe C dès les premières semaines de vie. |
 |
B - EPIDÉMIOLOGIE
- Habitat : Bactérie strictement humaine qui ne survit pas dans l'environnement. Le réservoir connu est le rhinopharynx de l'homme et 5 à 15% de la population en est porteur sain.
- Transmission par voie aérienne lors de contacts directs.
- Evolue en Europe sur un mode endémique (500 cas/an d'infections systémiques en France), avec un pic durant l'hiver. Le sérogroupe B est le plus fréquent (60%), puis C (40%). Les autres sérogroupes restent rares en France.

- Epidémique en Afrique: la ceinture méningée correspond globalement à l'Afrique entre les deux tropiques. Le sérogroupe A est le plus fréquent dans cette région du monde et survient sous forme d'épidémies. apparition depuis peu dans certaines régions d'Afrique d'épidémies d'infections à sérogroupe W135.
C - HISTOIRE NATURELLE DE L'INFECTION MÉNINGOCOCCIQUE
N. meningitidis est un commensal du nasopharynx de l'homme puisqu'une partie non négligeable de la population est porteur asymptomatique. Chez certaines personnes, essentiellement les jeunes nourrissons et les adolescents, la bactérie peut exercer son pouvoir pathogène, et disséminer dans le sang où elle sera à l'origine :
- soit d'une septicémie dont la forme la plus grave est le purpura fulminans (mortalité de 30% même traitée)
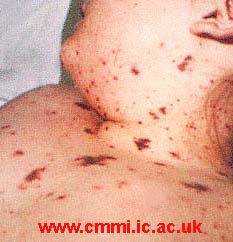
- soit d'une méningite après franchissement de la barrière hémato-méningée.
D - DIAGNOSTIC BACTÉRIOLOGIQUE
- Le diagnostic direct repose sur l'aspect morphologique, l'isolement et l'identification du germe:
- Hémoculture, LCR. Pas besoin de préciser la recherche de méningocoque.
- Autres prélèvements (prélèvement de gorge surtout, éventuellement prélèvement cutané en cas de purpura), mentionner dans la demande d'examen: "recherche de méningocoques", car ces prélèvements polymicrobiens nécessitent l'emploi de milieux spéciaux sélectifs.
- L'examen direct peut être évocateur : diplocoques à Gram-négatif à faces aplaties
Exemple: LCR purulent
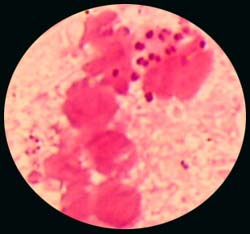
- Culture: Parmi les milieux utilisés figurent des milieux enrichis tel la gélose au sang cuit:
Exemple d'une courbe de croissance à N.meningitidis dans un automate d'hémoculture Bact'alert®
- L'identification biochimique et l'antibiogramme sont obtenus en 48-72 heures.
- La recherche d'antigènes solubles est possible (LCR, sang, urine).
- La possibilité de diagnostic par amplification génique (PCR) directement dans le liquide céphalo-rachidien existe.
- Il n'y a pas de diagnostic indirect (sérologie) .
E - TRAITEMENT - SENSIBILITÉ AUX ANTIBIOTIQUES
- Traitement curatif: Antibiothérapie qui repose sur les ß-lactamines dont l'amoxicilline (AMX), les céphalosporines de troisième génération (exemple: CTX, céfotaxime).
Cette espèce est généralement sensible à la rifampicine, aux macrolides dont l'érythromycine (E), ou encore au chloramphénicol (C).
Exemple d'antibiogramme après 24 h d'incubation à 37°C en présence de 5% de gaz carbonique
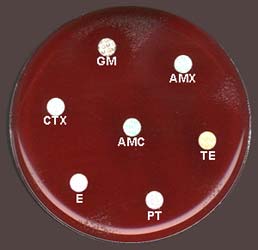
- Possibilité de moindre sensibilité à la pénicilline due à une modification d'affinité des protéines liant la pénicilline. Le céfotaxime et la ceftriaxone restent cependant des traitements de choix. De très rares souches produisent des bêta-lactamases, mais restent sensibles aux C3G.
F - PROPHYLAXIE : http://www.invs.sante.fr/beh/1990/9007/


Il existe un vaccin dont les indications sont les suivantes :
- vaccinations de masse lors d'épidémies à germe de sérogroupe A ou C
- vaccinations chez les sujets se rendant en zone de haute endémicité A ou W135 (Afrique intertropicale), surtout si séjour de longue durée.
- L'injection d'une dose après l'âge de 18 mois protège pour 3 ans contre les sérogroupes concernés.
Il n'y a pas de vaccination contre le sérogroupe B.
Il existe une antibioprophylaxie
TRES IMPORTANT
Dans les formes fulminantes, le pronostic reste très sévère et dépend de la précocité de la mise en route du traitement antibiotique, d'où les recommandations suivantes de la direction générale de la santé :
En dehors du milieu hospitalier, tout malade présentant des signes infectieux et à l'examen clinique, lorsqu'il a été totalement dénudé, un purpura comportant au moins un élément nécrotique de diamètre supérieur ou égal à 3 mm, doit immédiatement faire l'objet d'un traitement antibiotique parentéral approprié aux infections à méningocoques, de préférence par une céphalosporine de 3ème génération. Le malade doit être transféré d'urgence à l'hôpital. L'intervention d'une équipe médicalisée expérimentée (SMUR) est justifiée sous réserve que son délai d'intervention soit inférieur à 20 minutes. Dans tous les cas, les urgences de l'hôpital doivent être alertées de l'arrivée d'un cas suspect de purpura fulminans, afin que son accueil puisse être préparé.
Chimioprophylaxie
Dans l'entourage d'un malade (famille proche, pensionnaires d'une institution, soldats d'une caserne).
1er choix : rifampicine
- adulte : 600 mg/j pendant 2 jours
- enfant > 1 mois : 10 mg/kg/j pendant 2 jours
- enfant < 1 mois : 5 mg/kg/j pendant 2 jours.
2ème choix : si rifampicine contre-indiquée, spiramycine
- adulte : 2 g/j pendant 5 jours
- enfant : 50 mg/kg pendant 5 jours.
Critères de déclaration
L'infection méningococcique est une maladie à déclaration obligatoire si l'un au moins des critères de déclaration suivant est présent:
- Isolement bactériologique de méningocoques dans un site normalement stérile (sang, LCR, liquide articulaire, liquide pleural, liquide péricardique) ou à partir d'une lésion cutanée purpurique.
- Présence de diplocoque Gram négatif à l'examen direct du LCR.
- LCR évocateur de méningite bactérienne purulente (à l'exclusion de l'isolement d'une autre bactérie) et présence d'éléments purpuriques cutanés.
- LCR évocateur de méningite bactérienne purulente (à l'exclusion de l'isolement d'une autre bactérie) et présence d'antigène soluble méningococcique dans le LCR, le sang ou les urines ou d'une amplification génique positive.
- Présence d'un purpura fulminans (purpura extensif avec au moins un élément nécrotique de plus de 3 mm de diamètre associé à un syndrome infectieux sévère non attribué à une autre étiologie).
Remarques
- critères de déclaration = critères qui contrôlent la mise en route de la prophylaxie
- très clairement ces critères excluent les méningites à polynucléaires dont l'étiologie est inconnue.
NEISSERIA GONORRHOEAE
A - L'AGENT BACTÉRIEN
- Parfois appelé "gonocoque", agent de la blennorragie, de la gonoccie ou encore gonorrhée.
- Cocci à Gram négatif, phylogénétiquement très proche de N.meningitidis. Non capsulé.
- Très fragile dans le milieu extérieur, nécessite l'emploi de milieux de culture riches.
B - EPIDÉMIOLOGIE
- Strictement humain.
- 2ème cause d'urétrite après Chlamydia trachomatis.
C - HISTOIRE NATURELLE
Chez l'homme: urétrite le plus souvent aigue, épididymite + prostatite
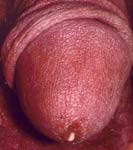
Chez la femme: urétrite et cervicite, passant souvent inaperçues
Dans les deux sexes:
- formes anorectales ou pharyngées (à rechercher systématiquement)
- conjonctivite
- gonococcémie et/ou infections disséminées (arthrites...) : associé à certaines souches
D - DIAGNOSTIC BACTÉRIOLOGIQUE
- Rechercher une éventuelle association avec Chlamydia ou d'autres germes de MST
- Effectuer, si nécessaire, la recherche chez le/les partenaire(s) sexuels
Diagnostic direct uniquement (mise en évidence du germe)
Prélèvements
- prélèvement uréthral et/ou sécrétions urétro-prostatiques après massage prostatique (dans les formes subaiguës)
- prélèvements anaux et pharyngés systématiques
Les prélèvements doivent être acheminés le plus rapidement possible au laboratoire, donc à ne pas conserver au réfrigérateur.
Examen direct - Culture
Examen direct: La présence de bactéries est recherchée soit par coloration de bleu de méthylène soit après coloration de Gram. L' élément pathonomonique est l'observation de germes intracellulaires au sein de polynucléaires.
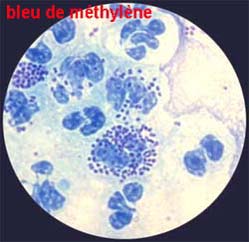
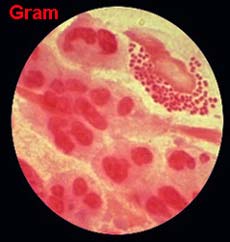
A la coloration de Gram, il s'agit de diplocoques à Gram négatif en forme de grain de café, le plus souvent associé à de nombreux polynucléaires dans les formes aigues.
La culture est indispensable sur des milieux riches et sélectifs (vancomycine par exemple). Le délai de croissance est en moyenne de 2 à 4 jours.

L'identification de cette espèce est biochimique après 24 h d'incubation à 37°C;
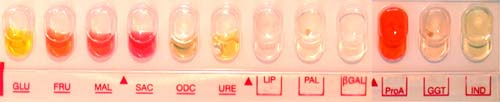
Il n'y a pas de diagnostic indirect (sérologie).
E - TRAITEMENT - SENSIBILITÉ AUX ANTIBIOTIQUES
Cette espèce est habituellement sensible à divers antibiotiques dont les ß-lactamines telles l'amoxicilline (AMX), son association avec l'acide clavulanique (AMC), les céphalosporines de troisième génération (exemple: CTX, céfotaxime); les tétracyclines (TE); la spectinomycine (SPT) ou encore les fluoroquinolones (exemple: CIP, ciprofloxacine).
La résistance acquise est variable selon les antibiotiques testés:
- ß-lactamines : nombreuses résistances plasmidiques (bêta-lactamases). Intérêt des C3G
- Tétracyclines : nombreuses résistances plasmidiques
- Fluoroquinolones: en augmentation.
Exemple d 'une souche résistante aux pénicillines (AMX), aux tétracyclines (TE),
aux quinolones (NA, acide nalidixique)
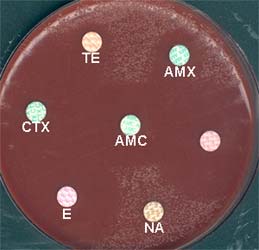
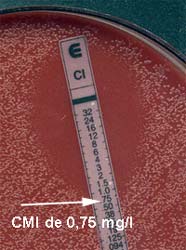
En cas de doute, la CMI pourra être précisée par le E-test (bandelette). Ré-évaluer le traitement initial à la lumière de l'antibiogramme
Ce cours a été préparé par le Dr. Ph. MORAND et le Professeur X. NASSIF (Faculté de Médecine Necker-Enfants Malades, PARIS V)
Quelques adresses:
http://neisseria.org/nm/
http://www.ands.dz/sap/infections-invasives2.htm
http://www.sante.gov.fr/
http://www.invs.sante.fr/beh/
http://www.lemonde.fr/article/0,5987,3244--291133-,00.html
http://www.caducee.net/DossierSpecialises/gyneco-obstetrique/gonorrhee1.asp
|
|
|
|
|