1 - Introduction
Le genre Helicobacter fait, comme les Campylobacters, partie des bactéries spiralées du tube digestif.
Il possède les caractères des bactéries spiralées du tube digestif, à savoir :
. Morphologie : forme spiralée ou incurvée
. Métabolisme : microaérobie et n'utilisant pas les sucres pour tirer son énergie.
. Ecologie : adapté à la vie dans le mucus.
Il est indivisualisable sur des critères génétiques : branche e des Protéobactéries.
Il existe de nombreuses espèces d'Hélicobacters (cf fiche diagnostique). Certaines sont gastriques, d'autres dites entéro-hépatiques.
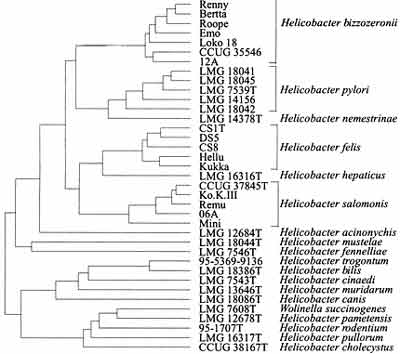
Helicobacter pylori cultivé depuis 1982 est l'espèce inféodée à l'homme à l'origine des ulcères et du cancer au niveau de l'estomac. Les deux découvreurs australiens de cette bactérie viennent d'être justement honorés du Prix Nobel:

http://nobelprize.org/medicine/laureates/2005/index.html
http://www.tallpoppies.net.au/cavalcade/warren.htm
2 - Maladies associées
La lésion de base de l'infection à H. pylori est une gastrite, c'est-à-dire une inflammation de la muqueuse gastrique qui a une définition histologique. Cette gastrite survient toujours quand H. pylori est présent. Elle peut persister des décennies, voire toute la vie du sujet sauf traitement intercurrent mais n'est pas forcément symptomatique. Par contre, elle peut évoluer vers les maladies suivantes :
. Maladie ulcéreuse
L'infection à H. pylori peut évoluer dans environ 5% des cas, vers la maladie ulcéreuse, autrefois considérée d'origine psychosomatique. Elle va fragiliser la muqueuse qui devient alors sensible à l'acide. L'éradication de H. pylori permet de guérir cette maladie.
. Cancer gastrique
L'infection à H. pylori est la première infection bactérienne associée au développement de cancers chez l'homme. Dans moins de 1% des cas, la gastrite va évoluer vers un carcinome gastrique. Cette évolution survient après plusieurs décennies et une séquence de transformations de la muqueuse où un état pré-cancéreux peut être observé. Ce cancer de mortalité élevée est encore la deuxième cause de mortalité par cancer dans le monde.
Un autre cancer de l'estomac : le lymphome du MALT (Mucosa Associated Lymphoid Tissue) encore plus rare a vu son pronostic transformé depuis la connaissance de H. pylori.
. Autres maladies
L'infection à H. pylori a été impliquée dans beaucoup d'autres maladies ou syndromes idiopathiques, avec des niveaux de preuve variables.
3 - Epidémiologie
H. pylori est une bactérie strictement humaine qui est transmise aux enfants en bas âge essentiellement dans le milieu familial. Sa transmission se fait par le liquide gastrique dans les pays développés suite à des vomissement ou régurgitations.
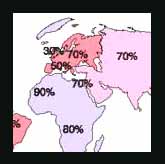
Dans les pays en développement, la voie fécale orale peut aussi être en jeu. La prévalence de l'infection dépend du niveau socio-économique. Actuellement on considère que 20 à 25% des adultes sont infectés en France, la prévalence augmentant de 20 à 70 ans. Chez les jeunes adultes autochtones la prévalence est <5%.
4 - Pathogénie
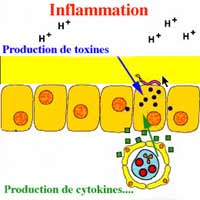
H. pylori a la capacité d'induire une réaction inflammatoire chez l'homme. Certaines souches possèdent un îlot de pathogénicité appelé cag qui code pour différents gènes formant un appareil de secrétion de type IV et d'autres molécules qui peuvent être injectées dans les cellules eucaryotes. Là elles peuvent entraîner un réarrangement de l'action et stimuler la production d'interleukine 8. Une cytotoxine dit VacA, car vacuolisante peut aussi être produite en quantité importantes par certaines souches.
On observe une augmentation de l'apoptose, de la prolifération cellulaire compensatrice et du risque de mutation en cas d'infection à H. pylori.
L'évolution de cette infection chronique va aussi dépendre de facteurs de l'hôte, notamment le polymorphisme de l'interleukine 1 b qui détermine le type de lésion qui va se développer, et de facteurs de l'environnement (tabagisme pour la maladie ulcéreuse, régime pauvre en vitamines et salé pour le cancer).
Le génome de trois souches a été séquencé et est actuellement l'objet de nombreuses recherches.
5 - Diagnostic (cf fiche de diagnostic)
Il met en jeu des méthodes invasives et non invasives.
1/ Les méthodes invasives nécessitent l'obtention de biopsies gastriques obtenues par fibroscopie. Elles sont au nombre de 4 :
| Examen histologique |
| Culture |
| Test à l'uréase |
| PCR |
. L'examen histologique est le plus classique. Il nécessite des prélèvements de bonne qualité et un observateur expérimenté. La détection de bactéries spiralées se fait en surface après coloration par Hématéine Eosine Safran (HES) ou Giemsa, voire par réaction immunoenzymatique.
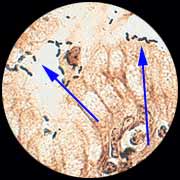
. La culture nécessite des conditions particulières de transport de la biopsie et un broyage. Elle est effectuée sur un milieu enrichi contenant des antibiotiques pour inhiber les contaminants, maintenu 7 jours à 37°C en atmosphère microaérobie. L'identification de H. pylori est basée sur des tests biochimiques (oxydase, catalase, uréase +). Elle permet l'étude de la sensibilité aux antibiotiques.

. Le test à l'uréase est un test spécial pour cette bactérie. Il est basé sur la production abondante d'uréase par H. pylori. Une biopsie où ces bactéries sont présentes mise dans un milieu contenant de l'urée, va l'hydrolyser en libérant de l'ammoniaque qui augmente le pH et fait virer un indicateur en 1 heure.

. La PCR peut aussi être utilisée pour détecter H. pylori avec des amorces basées sur l'ADNr 16S ou des gènes spécifiques (vacA comme ci-dessous).

2/ Les méthodes non invasives comprennent (cf fiche diagnostique):
| Sérologie | Détection d'antigènes | Test respiratoire |
* La sérologie utilise des extraits antigéniques et recherche en général, les IgG sériques par ELISA. La sensibilité et la spécificité varient selon les trousses commercialisées mais peuvent être excellentes. La spécificité peut être améliorée en pratiquant un immunoblot.
* Des tests immunoenzymatiques ont également été développés pour rechercher les antigènes de H. pylori dans les selles. Ils utilisent des anticorps poly ou monoclonaux.
* Le test respiratoire à l'urée ou analyse de l'air expiré consiste à faire absorber au patient de l'urée marquée au carbone 13 ou 12, puis à rechercher la présence ou l'absence de l'isotope dans le gaz carbonique expiré.
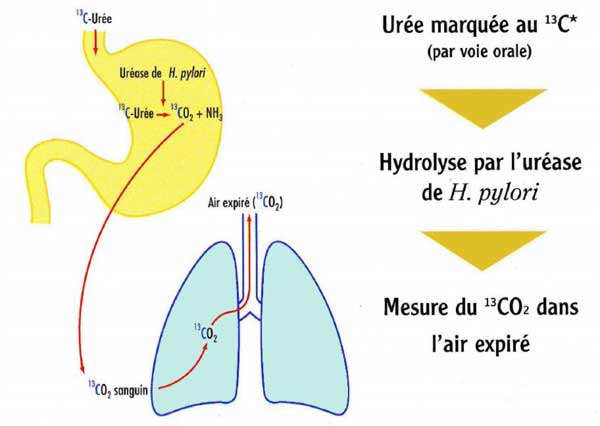
Si la bactérie est présente dans l'estomac, l'urée se scinde et libére le carbone 13 (ou 12) qui passe dans le sang puis les poumons et se retrouve dans l'air expiré. Ce test, fiable à plus de 98 %, présente l'avantage de rechercher la présence de la bactérie dans la totalité de l'estomac.
Le dépistage par le test respiratoire à l'urée marquée (C13*) est disponible en France (Helicobacter Test INFAI®) (http://www.vidal.fr/Medicament/helicobacter_test_infai-69959.htm). Le médecin prescrit le kit que le patient achète en pharmacie (de l'ordre de 35.57 euros) et apporte à un laboratoire d'analyses médicales (LABM) de son choix qui effectuera le prélèvement d'air expiré dont l'analyse finale sera effectuée après envoi postal à un laboratoire spécialisé: http://www.cnrch.u-bordeaux2.fr/ .
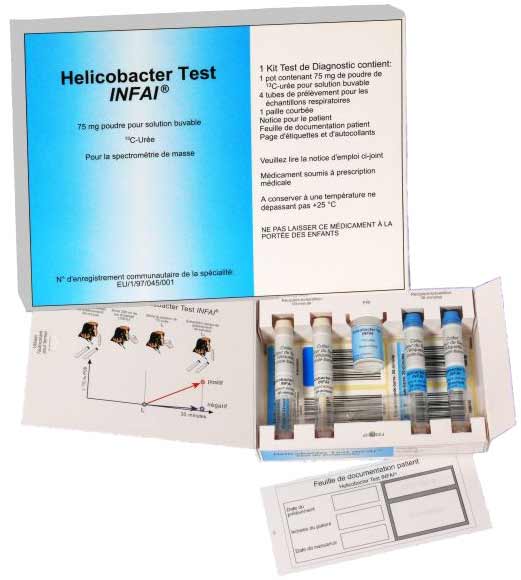
S'il est utile au dépistage, ce test peut également être utilisé pour contrôler l'efficacité du traitement.
6 - Traitement
- Le traitement recommandé pour éradiquer H. pylori associe un agent antisécrétoire (inhibiteur de la pompe à protons à double dose) à deux antibiotiques, amoxicilline et clarithromycine, durant 7 jours. En cas d'échec, une résistance à la clarithromycine est souvent en cause et cet antibiotique peut être remplacé par le métronidazole dans la tri-thérapie donnée alors durant 14 jours (antibiogramme, cf fiche de diagnostic).
La surveillance de l'efficacité du traitement est réalisée par un test respiratoire à l'urée marquée, 4 à 5 semaines après l'arrêt du traitement.
Les indications majeures pour l'éradication sont: la maladie ulcéreuse gastrique et duodénale, le lymphome gastrique du MALT et les lésions précancéreuses de l'estomac.
L'éradication à visée prophylactique pour le carcinome gastrique est actuellement en discussion.
Il n'y a pas actuellement de vaccin disponible.

http://www.cnrch.u-bordeaux2.fr/ (08.02.04)
http://nobelprize.org/medicine/laureates/2005/index.html
|
|
|
|
|