

| Objectifs du cours Faire la présentation d'une espèce bactérienne qui pourrait servir de modèle d'infections bactériennes communautaires provoquées - par des souches capsulées (de type b) ayant des propriétés invasives et responsables en particulier de méningites chez l'enfant et - par des souches non capsulées intervenant comme bactéries opportunistes dans des infections de l'appareil broncho-pulmonaire et de la sphère ORL de l'adulte (surinfection de bronchite chronique, sinusites) et de l'enfant (otite moyenne aiguë). |
1 - Introduction
La bactérie a été découverte par Pfeiffer, lors de l'épidémie de grippe des années 1890, dans les crachats de grippés. Pfeiffer en fait à tort à l'époque l'agent de la grippe (influenza) et la nomme Bacillus influenzae. Quelques années auparavant la même espèce avait été observée dans les sécrétions purulentes de sujets atteints de conjonctivite, en Egypte par Koch et aux USA par Weeks et nommée alors Bacillus aegyptius ou Bacille de Koch et Weeks. On retiendra : Germe de sortie lors d'infection virale (grippe, par exemple).
| Hôpital de campagne lors de l'épidémie de "fièvre espagnole" en 1918 aux USA (www.stanford.edu) | Moyen de protection chez des bénévoles australiens en 1918 |
 |
 |
Les besoins en facteurs de croissance, soupçonnés par Pfeiffer qui invente la gélose au sang (de pigeon), devenus les facteurs X pour inconnu (hémine) et V pour vitaminique (NAD) présents dans le sang, ont conduit à la dénomination moderne, Haemophilus influenzae.
Les Haemophilus aiment l'hème.
H. influenzae est une espèce classée dans le genre Haemophilus au sein de la famille des Pasteurellaceae.
 |
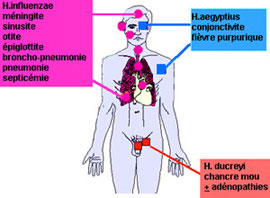 |
| Parmi ces espèces, seul H. ducreyi peut être considéré comme une bactérie pathogène spécifique, responsable du chancre mou, infection à transmission sexuelle. |
 |
2 - Caractères bactériologiques
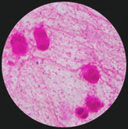
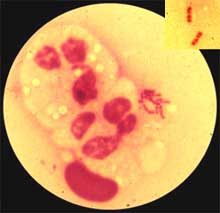
| H. influenzae se présente sous la forme de petits bacilles (coccobacilles) à Gram négatif. Il existe aussi des formes longues, traduisant un polymorphisme qui peut être observé dans certains produits pathologiques (liquide céphalo-rachidien). Exemples de coloration de Gram à partir d'une expectoration. |
 |
La culture se caractérise par l'exigence en facteurs de croissance intervenant dans les enzymes de la chaîne respiratoire, le facteur X ou hémine et le facteur V ou NAD présents dans le sang. Des milieux de culture particuliers, dits enrichis sont nécessaires comme la gélose "chocolat" supplémenté en X et V.
Exemples de culture sur une gélose au sang frais et une gélose chocolat après 24 h d'incubation à 37°C
 |
 |
Certaines souches possèdent une capsule polysaccharidique permettant de définir différents sérotypes, de a à f (décrits par Miss M. Pittmann en 1931). Le type b est le plus fréquent dont le polysaccharidique capsulaire est le polyribosylribitol phosphate (PRP).
3 - Habitat
H. influenzae fait partie de la flore normale des muqueuses des voies respiratoires supérieures de l'enfant et de l'adulte. La colonisation débute très tôt après la naissance et va se poursuivre tout au long de la vie. Dans une population donnée, de 40 à 60% d'enfants peuvent être porteurs d'H. influenzae (écouvillonnage nasopharyngé) et un "turn-over" des souches colonisantes a été montré. Les souches sont habituellement non capsulées. Le portage de souches capsulées, de type b ou d'autres sérotypes est peu fréquent, concernant moins de 5% des sujets, adultes ou enfants. Comme conséquence de la vaccination anti Hib, le portage de souches de type b a considérablement diminué, tendant vers la disparition.
La colonisation des muqueuses des voies respiratoires supérieures sera le point de départ, tant des manifestations invasives, que des infections opportunistes broncho-pulmonaires et ORL.
H. influenzae peut aussi coloniser la muqueuse vaginale, source possible de contamination et d'infections génitales et néonatales (dont l'évolution pourra être septicémique ou non).
4 - Pouvoir pathogène
H. influenzae est avant tout responsable d'infections communautaires de la sphère ORL de l'enfant et de l'adulte et de surinfections broncho-pulmonaires de l'adulte (plus rarement de l'enfant lors de différentes anomalies, dilatation de bronches, mucoviscidose). Ces infections sont provoquées par des souches non capsulées, exceptionnellement par des souches capsulées.
H. influenzae se place en tête ou partage avec le pneumocoque (parfois associés) cette première place et joue donc un rôle majeur dans une pathologie communautaire très fréquente (infection de tous les jours, de tout le monde, de tous les âges de la vie), quotidien du médecin praticien (de la ville et de la campagne !).
H. influenzae est aussi responsable de manifestations invasives, septicémiques avec différentes localisations, méningites, (les plus fréquentes 17 pour 100 000 enfants de moins de 5 ans avant la vaccination), mais aussi épiglottite, pneumonie, arthrite, péricardite, cellulite, et d'autres éventuelles localisations plus rares encore.
5 - Physiopathologie
Comme bactérie opportuniste, ou de surinfection, situation parfaitement décrite lors de la découverte du bacille, et retrouvée depuis, H. influenzae peut provoquer une infection localisée (oreille moyenne, sinus) lors de diminution des défenses locales, en particulier lors d'atteinte du système muco-ciliaire, après ou au cours d'une infection virale. D'autres facteurs physiques, chimiques ou toxiques (fumée du tabac) peuvent altérer les défenses de la muqueuse. H. influenzae possède aussi des éléments de surface (facteurs d'adhésion) ou des produits de sécrétions (IgA protéase) favorisant la colonisation et l'infection, mais dont le rôle n'a pas toujours été clairement démontré.
Dans la bronchite chronique, les altérations de la muqueuse et ses modifications, conjuguées avec d'autres facteurs, favorisent la colonisation puis la multiplication de différentes espèces bactériennes dont H. influenzae.
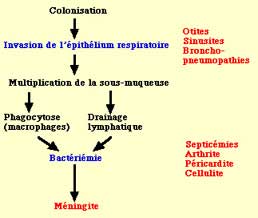 |
Lors de manifestation invasive, la capsule joue un rôle majeur. Le polysaccharide de capsule confère une protection contre la phagocytose et l'action lytique du complément. La virulence la plus forte est observée pour le type b, suivi par les types a, e et f. L'état septicémique s'installe après une première étape de colonisation puis de translocation conduisant à la traversée de la muqueuse et à la multiplication dans le tissu conjonctif et l'envahissement des petits vaisseaux. La multiplication sanguine résulte de l'action protectrice de la capsule contre la phagocytose et l'action du complément. |
| Les anticorps dirigés contre le polysaccharide de capsule (PRP du type b) sont protecteurs. Ils expliquent l'activité bactéricide du sérum. Ils apparaissent progressivement chez l'enfant. Cette activité bactéricide du sérum (et donc du rôle des anticorps) permet de comprendre les courbes de Fothergill et Wright qui ont montré en 1933, la relation existant entre l'activité bactéricide du sérum et l'incidence des méningites à H. influenzae de type b. | 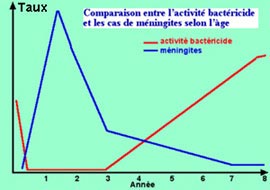 |
Le scénario épidémiologique classique, disparu depuis la vaccination, correspondait à une survenue plus fréquente des méningites entre 3 mois et 3 ans, période située entre la fin de la protection passive conférée par les anticorps d'origine maternelle et l'acquisition d'anticorps à un titre suffisant et protecteur (à partir de 3 ans).
La vaccination, utilisant un vaccin conjugué, a profondément modifié ce scénario classique et la vaccination, réalisable dès les premiers mois de la vie, confère une protection efficace.
6 - Diagnostic biologique
Le diagnostic biologique va reposer sur le seul diagnostic direct par mise en évidence de la bactérie après examen microscopique et après mise en culture. Il n'y a pas de diagnostic indirect, par sérologie, des infections à H. influenzae.
Comme pour tout diagnostic bactériologique, la qualité du prélèvement réalisé chez le patient va conditionner la qualité de l'examen et du résultat. Ceci est particulièrement vrai pour les prélèvements ouverts réalisés lors dinfections broncho-pulmonaires et O.R.L. Le seul examen bactériologique valable concernant les sécrétions bronchiques purulentes (lors de surinfection de bronchite chronique, de BPCO et surinfection de bronchite aiguë) est celui réalisé sur des sécrétions recueillies au lever, en fait lors de la toilette spontanée des bronches au réveil. Ainsi, les contaminations par la salive ou lors du passage au carrefour rhinopharyngé sont sans conséquences.
Les autres prélèvements: pus de sinus, écoulement spontané l'ors d'otite moyenne aiguë sont prélevés à l'écouvillon stérile.
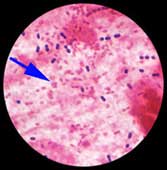
| L'examen microscopique est la première étape de l'examen bactériologique, réalisé avec ou sans coloration. La coloration de Gram permet de reconnaître de petits bacilles à Gram négatif, parfois polymorphes, associés à des formes longues (situation parfois retrouvée dans le LCR). Coloration de Gram d'une aspiration bronchique d'un malade en réanimation médicale (mélange avec S. pneumoniae) |
 |
Les milieux de culture doivent satisfaire les exigences de l'espèce et contenir les facteurs X et V. Les critères d'identification sont peu nombreux et la recherche des besoins en X et en V est une étape importante pour distinguer H.influenzae et H.parainfluenzae.
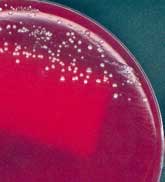
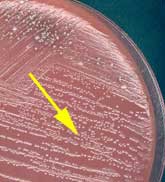
Aspiration sur gélose au sang frais et gélose chocolat et étude de l'exigence en facteurs X et V.
 |
 |
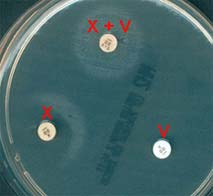 |
Les souches capsulées ont des colonies bombées, muqueuses et le type capsulaire est déterminé par agglutination sur lame à l'aide de sérums spécifiques ou par réaction de PCR avec des amorces spécifiques.
7 - Sensibilité aux antibiotiques
- H. influenzae est une espèce naturellement sensible à de nombreux antibiotiques:
* ß-lactamines telles pénicillines (amoxicilline, AMX), céphalosporines de 3 ème génération (céfotaxime, CTX)
* Phénicolés dont le chloramphénicol (C)
* Tétracyclines (T)
* Sulfamide seul (SSS) ou associé (SXT) au triméthoprime (TMP)
* Fluoroquinolones telle la ciprofloxacine (CIP)
Antibiogramme d'une souche par diffusion (méthode des disques)
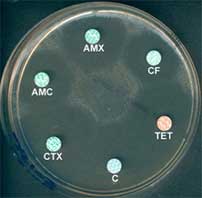 |
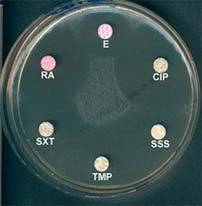 |
- La résistance naturelle concerne les macrolides comportant un cycle de 16 atomes, les lincosamines, la bacitracine, le mécillinam, l'oxacilline et les glycopeptides. C'est une espèce modérément sensible aux macrolides (cycle 14 et 15 atomes)(érythromycine ou ERY), les streptogramines, les céphalosporines de première génération (céfalotine ou CF).
Comme d'autres espèces bactériennes, H. influenzae est concerné par la résistance acquise touchant plusieurs familles d'antibiotiques.
* ß-lactamines: le mécanisme le plus fréquent est la production de bêta-lactamase (bla de type TEM). L'activité des aminopénicillines est restaurée en présence d'un inhibiteur de ß-lactamase. Un mécanisme non enzymatique est aussi observé reposant sur une modification de la cible des bêta-lactamines, les PLP ou protéines de liaison à la pénicilline, ayant subi des mutations ponctuelles entraînant des substitutions d'acides aminés et une diminution de l'affinité pour les bêta-lactamines. Ces PLP sont aussi les enzymes impliqués dans la synthèse dun composant de la paroi bactérienne, le peptidoglycane.
* La résistance acquise concerne la famille des tétracyclines (TET), des phénicolés (C), des fluoroquinolones ou encore le triméthoprime-sulfaméthoxazole (SXT), mais pour certains, l'incidence est très faible.
Résistance acquise (%) en France
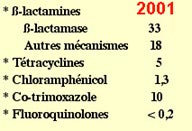 |
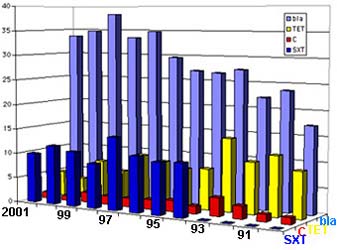 |
Ceci concerne l'ensemble des souches, toutes origines confondues. Dans certaines situations cliniques, la résistance peut être plus élevée, 45% de souches productrices de ß-lactamase parmi celles isolées de pus d'otite et de pus conjonctival.
Cette résistance aux antibiotiques concerne aussi les souches capsulées et invasives. Cependant, les souches résistantes restent accessibles à un traitement par céphalosporines de troisième génération injectables, par exemple céfotaxime, ceftriaxone (Conférence de Consensus:Traitement des méningites purulentes).
8 - Prophylaxie
H. influenzae fait partie de la flore normale des muqueuses colonisées par des souches non capsulées. Il faut donc vivre avec cette espèce bactérienne.
Les souches capsulées, en particulier le type b, sont (étaient) responsables de la grande majorité des manifestations invasives, en particulier les méningites. Sachant que les anticorps anticapsulaires sont des anticorps protecteurs (anti-PRP) (courbes de Fothergill et Wright de l'activité bactéricide du sérum selon l'âge), la vaccination à l'aide d'un vaccin à base de PRP purifié a été proposée dès la fin des années 1980. Mais ce vaccin polysaccharidique n'entraînait de protection que chez les enfants de plus de 2 ans, bien après le pic d'incidence de survenue des méningites (6 - 18 mois). Ce polysaccharide purifié est un antigène thymo-indépendant. Sous forme de vaccin conjugué, le PRP associé à une protéine devient thymo-dépendant et protecteur dès les premiers mois de la vie, utilisable chez le nourrisson dès 2 mois.
 |
La prophylaxie des infections à type b, en particulier les méningites, repose sur l'utilisation dun vaccin conjugué (PRP-, T pour anatoxine tétanique ; 3 injections à 1 mois d'intervalle, avant 6 mois, suivies d'un rappel à 18 mois). Ce vaccin, par son efficacité, peut être considéré comme le meilleur apport dans le domaine des infections bactériennes et des vaccinations antibactériennes depuis la mise au point des anatoxines (tétanique et diphtérique) dans les années 1920. |
Dans les pays où la vaccination est généralisée, les méningites à type b ont pratiquement disparu, avec dans le même temps, une quasi disparition du portage des souches de type b. La question est posée de l'avenir des autres types capsulaires d'Haemophilus influenzae. A ce jour, aucun autre type n'a pris la place du type b. |
Ce cours a été préparé par le Professeur H. DABERNAT (Faculté de Médecine Toulouse - Purpan))(Novembre 2002)
Pour en savoir plus :

Quelques adresses:
http://www.chu-rouen.fr/ssf/pathol/haemophilusinfection.html
|
|
|
|
|